Gevangen in je eigen lichaam.
Gevangen in je eigen lichaam.
Beeld je in dat je niet meer kan bewegen. Je ligt volledig stil op je bed en kan enkel nog rond je kijken. Praten gaat moeizaam. Ademen ga at moeizaam. Je hebt jeuk maar je kan er niet bij. Je hebt dorst maar je kan het glas water niet grijpen. Je zit gevangen in een lichaam vol pijn. Wanneer je gediagnosticeerd wordt met Amyotrofe Laterale Sclerose, afgekort als ALS, is dit het vooruitzicht. Een doeltreffende behandeling is er tot op vandaag niet. ALS hebben is meer dan een doodsvonnis. Het is een lijdensweg.
at moeizaam. Je hebt jeuk maar je kan er niet bij. Je hebt dorst maar je kan het glas water niet grijpen. Je zit gevangen in een lichaam vol pijn. Wanneer je gediagnosticeerd wordt met Amyotrofe Laterale Sclerose, afgekort als ALS, is dit het vooruitzicht. Een doeltreffende behandeling is er tot op vandaag niet. ALS hebben is meer dan een doodsvonnis. Het is een lijdensweg.
Wereldwijd worden elke dag 328 mensen gediagnosticeerd met ALS. De ziekte treft zowel mannen als vrouwen, met een gemiddeld leeftijd van 55 jaar oud maar er zijn ook tieners met ALS. Deze patiënten ondervinden krachtverlies en worden vervolgens geleidelijk aan verlamd. De oorzaak is het verlies van zenuwcellen die instaan voor de motoriek (motorneuronen genoemd). Deze cellen zorgen voor de signaaloverdracht tussen de hersenen en de spieren. Zonder motorneuronen zijn je spieren nog intact en heb je wel de wil om te bewegen, maar het commando zal jouw spieren niet bereiken (Fig. 1). Alles wat je bent en kan sijpelt langzaamaan weg. Het merendeel van de ALS-patiënten sterft binnen twee tot vijf jaar doordat ook de ademhalingspieren verlammen. Kortom, ze stikken. Op dit moment is er geen eenduidige hypothese die het verlies aan motorneuronen volledig kan verklaren. Dit bemoeilijkt de ontwikkeling van een doeltreffend geneesmiddel. Daarom is wetenschappelijk onderzoek naar waarom en hoe deze motorneuronen afsterven noodzakelijk.
Zal ontsnapping ooit mogelijk zijn?
Zenuwcellen van ALS-patiënten zijn enkel in een beperkte hoeveelheid beschikbaar. Daarom worden er dierenmodellen, zoals vliegen, vissen en muizen gebruikt voor wetenschappelijk onderzoek. Jarenlang onderzoek met deze modellen heeft onze kennis over ALS vergroot maar heeft tot op vandaag niet kunnen leiden tot een geneesmiddel die de ziekte stopt. Eén van de oorzaken is dat ALS-patiënten en ziektemodellen niet identiek zijn. Ten eerste, dieren verschillen van mensen. Bovendien is de complexiteit van de ontwikkeling van deze ziekte in mensen niet volledig aanwezig. In deze dierenmodellen ontwikkeld ALS zich artificieel door het aanbrengen van een genetisch wijziging (een mutatie) in slechts één gen. Dit is in overeenkomst met een kleine groep van ALS-patiënten maar is verschillend van de oorzaak van ALS in de meeste patiënten. Er wordt verondersteld dat in deze groep een complexe combinatie van meerdere genen en omgevingsfactoren een rol speelt in het ziekteproces.
Het gebruik van geïnduceerde pluripotente stamcellen (iPSCn) biedt ons hier een oplossing aan. Hiervoor vertrekken we vanuit de huidcellen van ALS-patiënten (Fig.2). Het voordeel is dat huidcellen op een eenvoudige manier kunnen verkregen worden in tegenstelling tot zenuwcellen. Vervolgens worden deze huidcellen terug getransformeerd naar een “basiscel”, namelijk stamcellen. Deze stamcellen gekend als iPSCn hebben de mogelijkheid om, wanneer blootgesteld aan de juiste factoren, elke soort cel in het menselijke lichaam te vormen. In onze studie werd aangetoond dat deze stamcellen succesvol kunnen worden omgezet in motorneuronen, de cellen die afsterven bij ALS. Dit is in overeenkomst met andere studies en heeft ons de mogelijkheid om te werken met menselijke weefsels, in de plaats van dierenmodellen.
Figuur 1. Bron: the Inspiration room; ALS-campagne “No signal in Canada”. Fotograaf Russell Monk en Ben Weeks.
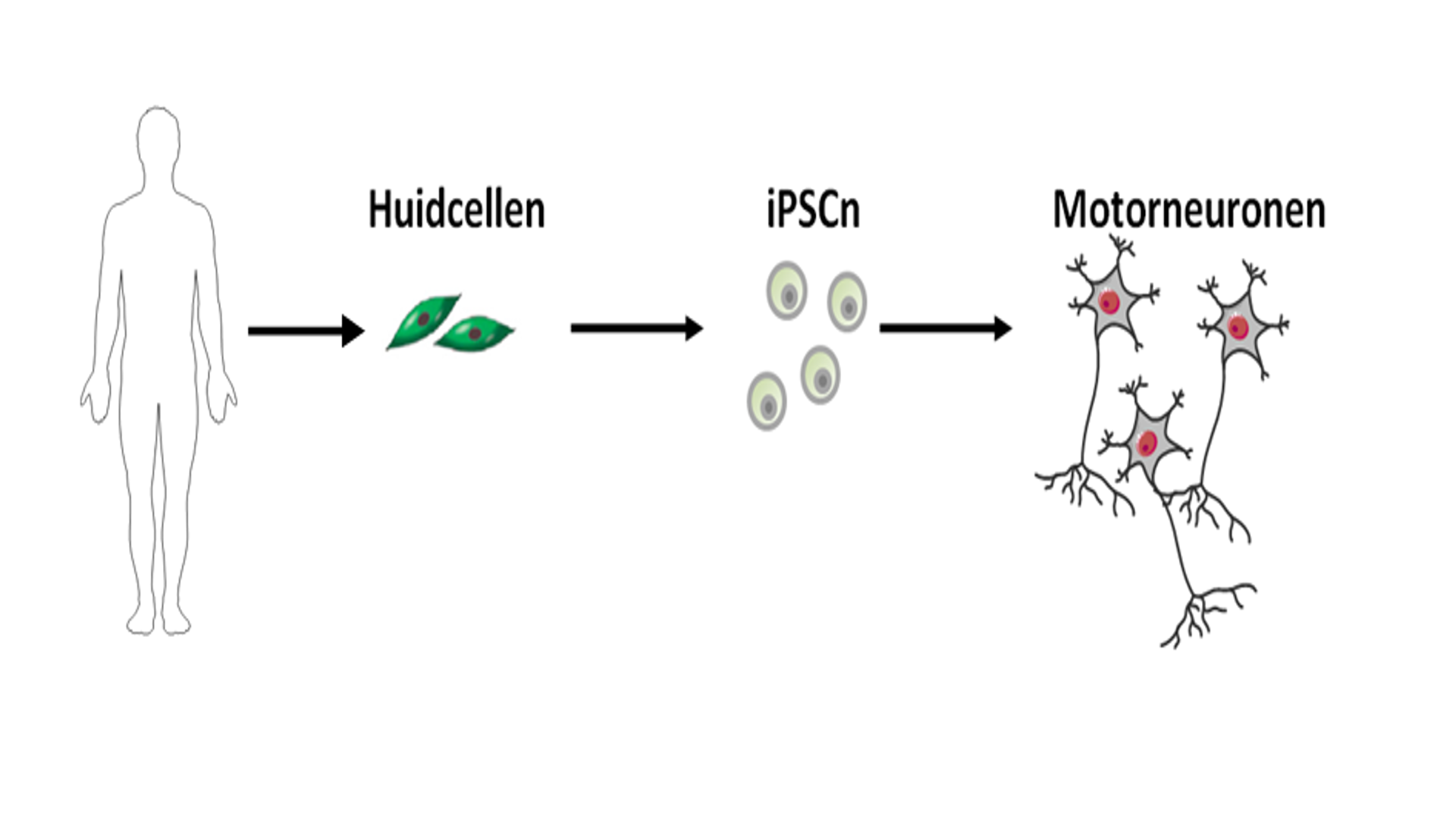
Figuur 2. De huidcellen van ALS-patiënten worden gebruikt om via een tussenstap van geïnduceerde pluripotente stamcellen (iPSCn) motorneuronen te ontwikkelen. Motorneuronen zijn de belangrijkste cellen in het ALS-onderzoek omdat deze cellen afsterven bij ALS-patiënten. Motorneuronen rechtstreek verkrijgen van de patiënten is een schadelijke en niet efficiënte methode. Bron figuren: medical servier.
Maar er is meer! Er werden verschillen opgemerkt tussen motorneuronen afkomstig van ALS-patiënten en motorneuronen afkomstig van gezonde personen. Een motorneuron bestaat uit een klein cellichaam en een erg lange uitloper, die het axon wordt genoemd (Fig. 3). Het cellichaam is het “hart” van het neuron waar nieuwe elementen worden aangemaakt en afgebroken. Het kan worden opgedeeld in de kern en het omliggende cytoplasma (Fig. 3). Het axon zorgt voor de verbinding tussen de hersenen (waar het cellichaam ligt) en de spieren. Een axon kan in het menselijke lichaam meer dan 1 meter lang zijn! Daarom is transport langs dit axon essentieel voor een goede gezondheid van het motorneuron. Goede elementen worden zo verdeeld over het lange axon en beschadigde elementen worden afgevoerd naar het cellichaam voor hun afbraak. Onze studies wezen erop dat er een verstoring is van dit axonaal transport. Naast dit verstoord transport werd ook een mislocalisatie waargenomen van een bekend ALS-geassocieerd eiwit, namelijk FUS (Fused in Sarcoma). FUS is normaal sterk aanwezig in de kern van het cellichaam. Echter, in de ALS-cellijnen werd een hogere aanwezigheid van FUS waargenomen in het cytoplasma (Fig. 4), wat een negatief effect kan hebben op het motorneuron.
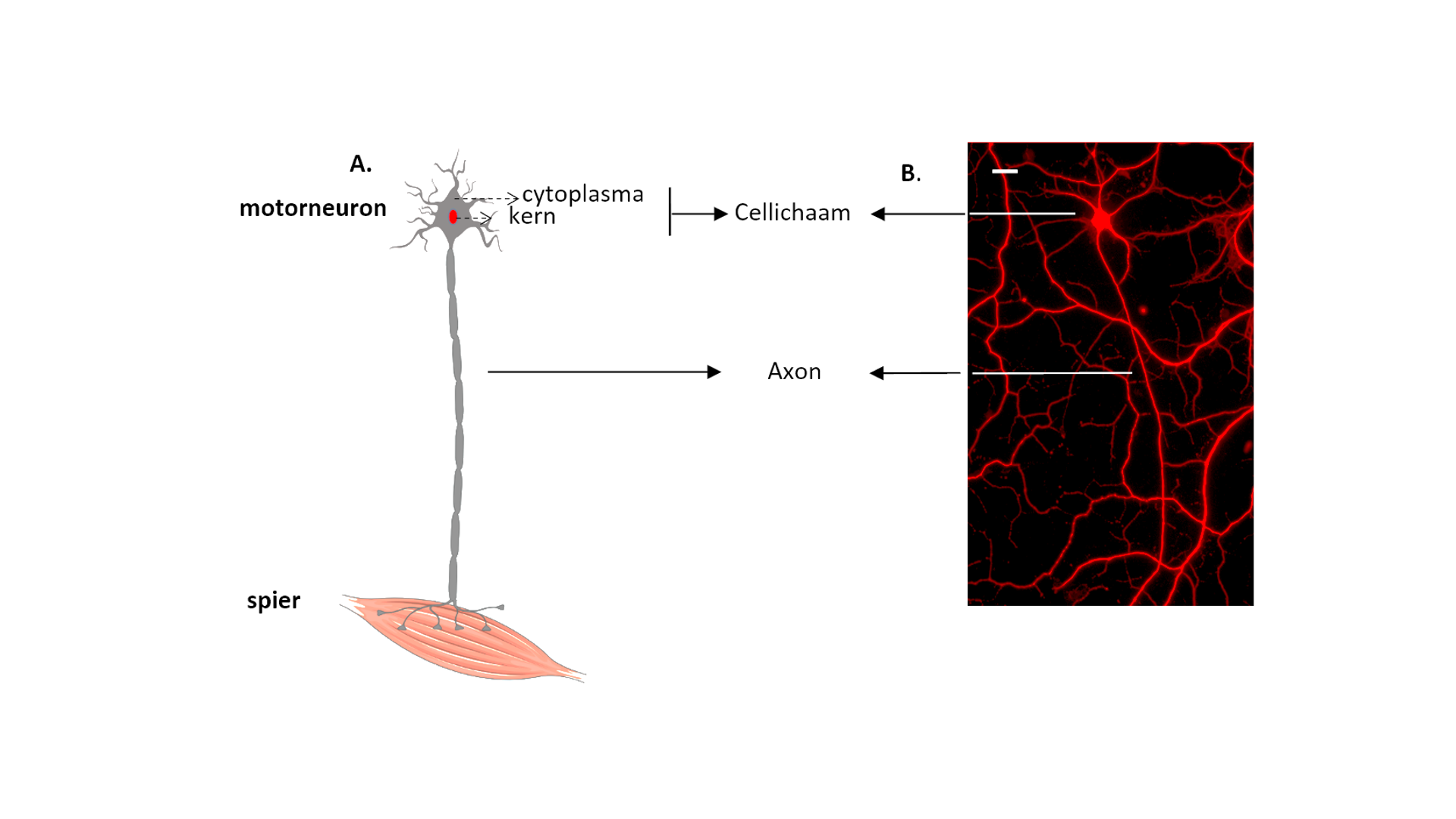
Figuur 3. Het motorneuron. (A) Een schematische weergave van een motorneuron en (B) een met fluorescent gemerkte motorneuron verkregen vanuit iPSCn. (A) Bron figuur: medical servier (B) Schaalbar= 20 µm.
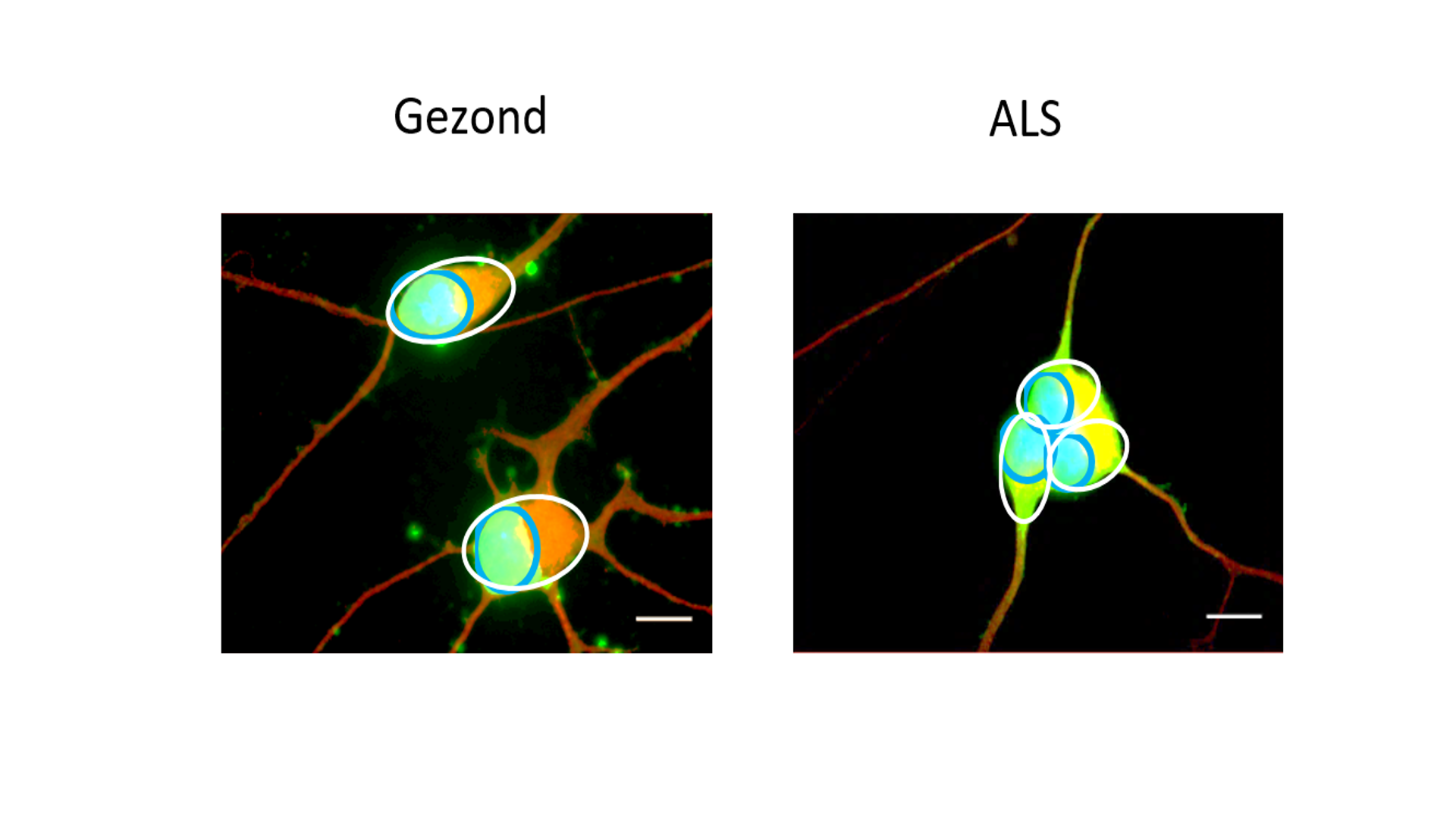
Figuur 4. FUS mislocalisatie. iPSC-afgeleide motorneuronen van een gezonde persoon en een ALS-patiënt gemerkt met fluorescente merkers. Rood = het motorneuron. Blauw= de kern; omgeven door een blauwe cirkel. Het cytoplasma is omgeven door een witte cirkel. Groen= FUS. Geel= overlap tussen het cytoplasma en FUS. Merk op dat FUS meer gelocaliseerd is in het cytoplasma (gele kleur) bij de motorneuronen afgeleid van de ALS-patiënt. Schaalbar= 40 µm.
Veel werk moet er nog worden verzet voordat wetenschappers een duidelijk beeld zullen hebben over wat er precies fout loopt. Hoopvol is dat de opkomst van iPSCn een nieuwe wind brengt door het ALS-onderzoek. Deze nieuwe inzichten leiden dan misschien wel tot de ontwikkeling van een geneesmiddel die de ziekte stopt of zelfs geneest, zodat de mensen getroffen door ALS niet langer gevangen zullen zitten in hun eigen lichaam.









