Artificiële intelligentie doorgrondt ons immuunsysteem
Het immuunsysteem beschermt ons tegen allerhande pathogenen – bacteriën, virussen, etc. Het is echter niet opgewassen tegen elke indringer. Er is bijvoorbeeld nog steeds geen geneesmiddel voor het HIV-virus dat in 2016 nog 1 miljoen levens eiste (WHO, 2017). Blijvend onderzoek naar het immuunsysteem is dus van belang. Een nieuwe techniek die ons gedetailleerde inzichten kan verschaffen in dit systeem is afbeeldingsflowcytometrie. In mijn scriptie werd deze techniek met artificiële intelligentie gecombineerd.
Het immuunsysteem is een erg complex geheel van cellen en mechanismen dat een organisme beschermt tegen allerlei indringers of pathogenen waaronder virussen en bacteriën. Om dit te bereiken beschikt het immuunsysteem over een groot arsenaal van cellen die zich voornamelijk in het bloed bevinden. Elke cel in dit systeem is van een bepaald type, en elk type cel heeft een specifieke functie. Zo zijn er bijvoorbeeld de neutrofielen die snel reageren na een ontsteking, de T-helpercellen die vechten tegen infecties, en nog tientallen andere types.
Er zijn echter nog heel wat pathogenen waar het immuunsysteem niet tegen is opgewassen. Denk bijvoorbeeld aan het eerder vermelde HIV-virus. Dit virus verzwakt het immuunsysteem zodat het ons niet langer kan beschermen tegen een griepje of verkoudheid. We noemen dit immunodeficiëntie. Het immuunsysteem reageert ook zonder infecties niet altijd foutloos. Het kan bijvoorbeeld een allergische reactie teweeg brengen wanneer het te heftig reageert op bepaalde onschadelijke prikkels, zoals een wespensteek of pollen bij iemand met hooikoorts.
Immuuncellen onder de loep
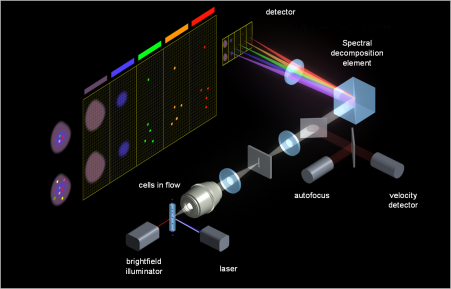 Om deze ziektes en kwalen de wereld uit te helpen, moeten we het immuunsysteem volledig doorgronden en karakteriseren. Dit wordt onderzocht in het domein van de immunologie waarin mijn onderzoek zich ook bevindt. In mijn scriptie onderzocht ik een techniek om met artificiële intelligentie immuuncellen te classificeren op basis van afbeeldingen ervan, gemaakt door een afbeeldingsflowcytometer (Figuur 1). Zo’n instrument fotografeert duizenden cellen per seconde met hoge precisie en verzamelt zo veel informatie over de cellen in een bloedstaal van een patiënt, bijvoorbeeld. Door de afbeeldingen te verwerken met artificiële intelligentie kunnen we uit die hoop informatie ook heel wat afleiden over het immuunsysteem van een patiënt.
Om deze ziektes en kwalen de wereld uit te helpen, moeten we het immuunsysteem volledig doorgronden en karakteriseren. Dit wordt onderzocht in het domein van de immunologie waarin mijn onderzoek zich ook bevindt. In mijn scriptie onderzocht ik een techniek om met artificiële intelligentie immuuncellen te classificeren op basis van afbeeldingen ervan, gemaakt door een afbeeldingsflowcytometer (Figuur 1). Zo’n instrument fotografeert duizenden cellen per seconde met hoge precisie en verzamelt zo veel informatie over de cellen in een bloedstaal van een patiënt, bijvoorbeeld. Door de afbeeldingen te verwerken met artificiële intelligentie kunnen we uit die hoop informatie ook heel wat afleiden over het immuunsysteem van een patiënt.
Een afbeeldingsflowcytometer kan twee types afbeeldingen maken van een cel. Enerzijds zijn er de label-vrije afbeeldingen (eerste tot derde afbeelding in Figuur 2), en anderzijds de fluorescentie afbeeldingen (vierde tot laatste afbeelding in Figuur 2). In het eerste type afbeeldingen wordt de vorm en het uitzicht van de cel vastgelegd met een soort microscoop. Voor het tweede type afbeeldingen moeten er eerst fluorescente labels aangebracht worden op de cellen. Die labels geven fluorescent licht af van een specifieke kleur wanneer de cellen gefotografeerd worden. Aan de hand van de specifieke kleur kunnen we dan vaststellen van welk type de cel is. We geven een cel als het ware een fluorescerend hesje om ze sneller en makkelijker te kunnen herkennen en classificeren. Deze labels zijn echter duur en ze aanbrengen op de cellen is een complex en arbeidsintensief proces.

Efficiënter (ver)werken met artificiële intelligentie
In het beste geval gebruiken we dus enkel de label-vrije afbeeldingen om de cel-classificatie uit te voeren. Wanneer we dit doen, beschikken we echter over heel wat minder informatie om de cellen te herkennen, wat een manuele classificatie onmogelijk maakt. In mijn scriptie heb ik onderzocht of een algoritme er toch nog in kan slagen om de cellen juist te sorteren. Hiervoor werden een aantal technieken uit de artificiële intelligentie toegepast.
De gebruikte technieken vallen onder de noemer van machine learning. Bij dit soort technieken leert een algoritme zelf regels om bijvoorbeeld een onderscheid te kunnen maken tussen cellen op basis van subtiele karakteristieken van deze cellen. Deze karakteristieken kunnen bijvoorbeeld de diameter van een cel of dikte van de celwand zijn. Om de regels te leren moet het algoritme een groot aantal voorbeelden te zien krijgen. Deze voorbeelden moeten ook gelabeld zijn – niet te verwarren met de fluorescente labels van eerder –, wat betekent dat we het algoritme moeten vertellen dat het naar een T-helpercel kijkt bijvoorbeeld.
Genoeg voorbeelden van elke celtype verzamelen bleek in dit onderzoek een grote uitdaging te zijn: de meting van de cellen is duur en tijdrovend, en sommige celtypes zijn simpelweg minder frequent aanwezig in het bloed. Om toch genoeg afbeeldingen te kunnen voorleggen aan het algoritme werd data augmentatie toegepast. Dit houdt in dat originele metingen van cellen willekeurig aangepast worden, bijvoorbeeld door de diameter van de cel iets te verhogen of verlagen. Op die manier worden zogezegd nieuwe cellen gecreëerd die als input aan het algoritme getoond kunnen worden.
Deze resultaten zijn zonder twijfel beter dan wat een wetenschapper manueel zou kunnen behalen
In dit onderzoek werden miljoenen label-vrije afbeeldingen van cellen aan een aantal verschillende machine learning algoritmen getoond. De geteste algoritmen presteren heel goed voor bepaalde celtypes. Wanneer we een algoritme cellen tonen van een nieuw bloedstaal is het in staat om minstens 95% van deze cellen juist te classificeren. Deze resultaten zijn zonder twijfel beter dan wat een wetenschapper manueel zou kunnen behalen, gezien de label-vrije afbeeldingen van verschillende celtypes onmogelijk met het blote oog te onderscheiden zijn.
Samengevat toonde dit onderzoek aan dat door artificiële intelligentie toe te passen in bepaalde immunologie-onderzoeken, het toevoegen van fluorescente labels niet langer nodig is. Dit is een interessante vondst die immunologie toegankelijker en efficiënter maakt. Dit onderzoek wordt ook verder gezet in mijn doctoraat waar ik nog meer technieken uit de artificiële intelligentie zal toepassen om nog meer voordeel te halen uit de veelbelovende afbeeldingsflowcytometrie.









